
| Главная | ||||
| Advertisements | ||||
| Фармацевтические технологии и упаковка | ||||
| Медтехника. Лекарства, изделия медназначения. Дезсредства | ||||
| Стоматолог-практик | ||||
| Статьи Фармацевтические технологии и упаковка - Лекарства по GMP | ||||
| Статьи Медтехника. Лекарства, изделия медназначения. Дезсредства | ||||
| Подписка | ||||
| Рекламодателям | ||||
| Контакты | ||||
Фармакотехнологическое исследование мягких лекарственных форм и космецевтических гелей
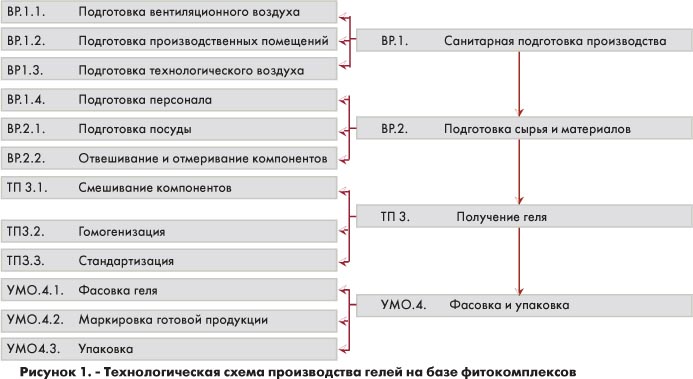
К.А.Курбанова, аспирант С.В. Москаленко, К.А. Эбзеева, научный руководитель - профессор Э.Ф. Степанова, Пятигорская государственная фармацевтическая академия, г. Пятигорск Современные фитопрепараты обладают рядом несомненных достоинств: они широко используются в комплексной терапии различных заболеваний, обладая низкой токсичностью, изотоничностью при трансдермальном применении, широким спектром действия, способностью к сочетанию с дженериками. В этом поиск природных объектов и разработка на их основе корригированных лекарственных препаратов является перспективным направлением. Целью наших исследований явилась разработка лекарственных форм и космецевтических средств, содержащих фитокомплексы растений, имеющих неограниченную сырьевую базу и исследование их фармакологического действия. Этими объектами служили фитокомплексы лавра благородного, мелиссы, пастушьей сумки обыкновенной, каштана конского, донника лекарственного. Нами предложена технология гелей с использованием в качестве гелеобразующей основы карбопола-940. Основные этапы производства и технологическая схема представлены на рисунке 1.
Особенностями данной технологической схемы являются этапы ТП 3.1. - смешивание компонентов и ТП 3.2. - гомогенизация. Для производства геля мы рекомендуем использовать реактор-смеситель соответствующей емкости для компонентов с вязкостью - 200 н/см2 , для гомогенизации геля мы предлагаем использовать РПА традиционной конструкции. Весь технологический процесс мы предлагаем проводить в периодическом варианте. При получении гелей в качестве действующих компонентов вводили либо соответствующие спиртовые экстракты, полученные с использованием спирта разной концентрации, либо липосомальную эмульсию, полученную на базе этих же экстрактов. Получение липосомальной эмульсии проводили традиционно, вводя экстракты в оболочку и полость везикул методом «замораживания-оттаивания». Методика выполнялась следующим образом: К липидной пленке, состоящей из фосфатидилхолина и холестерина в соотношении 3:1, добавляют иммобилизируемое вещество в 0,14 М растворе маннита из расчета 1 мл на 100 мл липидов. Если использование маннита является нежелательным, то могут применяться другие креопротекторы, например холинхлорид. Смесь встряхивают и подвергают при охлаждении ультразвуковой обработке в течение 3 минут с частотой 22 кГц. Полученные липосомы вместе с невключившимся в них препаратом быстро замораживают в жидком азоте, после чего оттаивают, погружая емкость с препаратом в воду комнатной температуры. Процедуру замораживания-оттаивания повторяют 6 раз. К размороженной последний раз смеси добавляют 4-кратный объем 0,14 М раствора хлорида натрия, в котором суспендируют полученные большие моноламеллярные липосомы. Об эффективности иммобилизации гидрофобных веществ судили, определяя стабильность эмульсии путём микроскопирования, с использованием окраски Суданом III полуколичественно в баллах. Поле зрения ограничивалось окулярной сеткой. Критерии оценки: - 0 баллов (отсутствие окраски), очень слабое окрашивание - 1 балл, слабое окрашивание - 2 балла, умеренное окрашивание - 3 балла, 4 балла - сильное окрашивание. Для достоверности полученных данных проводили статистическую обработку с использованием критерия х2 Пирсона (Романенко A.M., Сватков В.И., 1975). Если величина оказывалась больше или равна 0,05, то нулевая гипотеза при данном числе степени свободы не отвергалась. Таким образом было установлено, что в разработанных мягких лекарственных формах содержание гидрофобных веществ соответствовало этому критерию.
В опытах на белых крысах была установлена анальгезирующая активность этих лекарственных форм. После наложения разности потенциалов на верхнюю треть хвоста животных ниже и выше места наложения гелей изменялся порог чувствительности, при котором наступал тремор хвоста, попытка сбросить электрод, вокализация. Данные эксперимента представлены на рисунке 3. Как видно из данного рисунка, напряжения, при которых возникал тремор хвоста, вокализация и попытка сбросить электрод повышались на 40,0% (р<0,05), 34,65 (р<0,05) и 25,0% (р<0,005) по сравнению с контролем, которым служила гелевая основа. Гель пастушьей сумки достоверно не изменял порог болевой чувствительности. Таким образом, полученные экспериментальные данные позволяют судить о перспективности использования гелей мелиссы и пастушьей сумки для коррекции воспалительных процессов в комплексной терапии.
Известно, что наличие прооксидантного эффекта обуславливает один из факторов, способствующих заживлению ран за счет ускорения обновления клеточных мембран, стимулирования роста быстропролиферирующих тканей. В результате эксперимента по ранозаживляющему действию, регистрируемого ранотензиометрически, было установлено, что под влиянием мази повысилась прочность рубца на 111,5% (р<0,05) по сравнению с контролем - животными, не подвергавшимися санации. Таким образом, было установлено, что мазь с экстрактом донника обладает ранозаживляющим действием и может быть использована как космецевтическое средство.
Под влиянием липосомального геля донника происходило торможение развития травматического отёка в более ранние сроки, чем при применении традиционного препарата - 2% геля троксевазина. Выводы Таким образом, исследование космецевтических гелей, полученных на основе различных растительных объектов, позволяет заключить, что одним из механизмов биологической активности исследованных объектов является их влияние на процессы свободнорадикального окисления, то есть как антиоксидантное, так и прооксидантное действие. Эти результаты могут быть использованы в методологии исследовательского поиска при разработке аналогичных космецевтических средств. |
| Дизайн webing.ru |
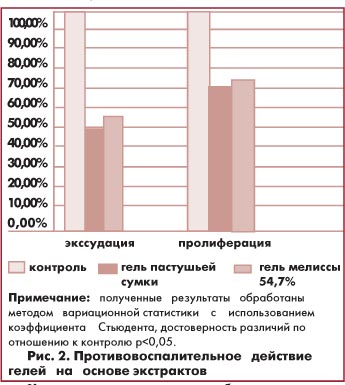 Для оценки фармакологического эффекта липосомального геля (действующие компоненты - экстракты лавра и донника) изучали его влияние на динамику травматического отека и отека, вызванного острым веностазом. Биологическую активность традиционных гелей с экстрактами мелиссы, пастушьей сумки исследовали по влиянию на уровень перекисного окисления липидов и стабильность биомембран. Определялась противовоспалительная и анальгезирующая активность лекарственных форм с указанными экстрактами. На моделях пероксидного и кислотного гемолиза эритроцитов крыс in vitro (Mizushima Y., Sokai S., 1970) было установлено, что экстракты из мелиссы и пастушьей сумки обладают прооксидантными свойствами. У экстракта мелиссы процент перекисного и кислотного гемолиза был выше, чем в контроле на 75,0% и 30,0% соответственно, а у экстракта пастушьей сумки - на 60,0% и 33,3% в сравнении с контролем, которым служил физиологический фосфатный буфер. Была установлена противовоспалительная активность гелей на базе экстрактов на модели асептического воспаления, вызванного имплантацией чужеродного тела у крыс (методические рекомендации Фармакологического комитета МЗ СССР, 1983), как на стадии пролиферации, так и на стадии экссудации. Гель с экстрактом из пастушьей сумки проявил себя активнее в процессе подавления воспаления и коррелировал с гелем мелиссы. При использовании геля пастушьей сумки интенсивность экссудации снизилась по сравнению с контролем, которым служили нелеченные животные, с одновременным снижением пролиферативного воспаления. Сходные результаты получены при применении геля мелиссы. Экспериментальные данные представлены на рисунке 2.
Для оценки фармакологического эффекта липосомального геля (действующие компоненты - экстракты лавра и донника) изучали его влияние на динамику травматического отека и отека, вызванного острым веностазом. Биологическую активность традиционных гелей с экстрактами мелиссы, пастушьей сумки исследовали по влиянию на уровень перекисного окисления липидов и стабильность биомембран. Определялась противовоспалительная и анальгезирующая активность лекарственных форм с указанными экстрактами. На моделях пероксидного и кислотного гемолиза эритроцитов крыс in vitro (Mizushima Y., Sokai S., 1970) было установлено, что экстракты из мелиссы и пастушьей сумки обладают прооксидантными свойствами. У экстракта мелиссы процент перекисного и кислотного гемолиза был выше, чем в контроле на 75,0% и 30,0% соответственно, а у экстракта пастушьей сумки - на 60,0% и 33,3% в сравнении с контролем, которым служил физиологический фосфатный буфер. Была установлена противовоспалительная активность гелей на базе экстрактов на модели асептического воспаления, вызванного имплантацией чужеродного тела у крыс (методические рекомендации Фармакологического комитета МЗ СССР, 1983), как на стадии пролиферации, так и на стадии экссудации. Гель с экстрактом из пастушьей сумки проявил себя активнее в процессе подавления воспаления и коррелировал с гелем мелиссы. При использовании геля пастушьей сумки интенсивность экссудации снизилась по сравнению с контролем, которым служили нелеченные животные, с одновременным снижением пролиферативного воспаления. Сходные результаты получены при применении геля мелиссы. Экспериментальные данные представлены на рисунке 2.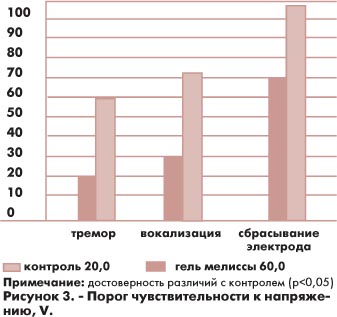 Как видно из гистограммы, обе лекарственные формы проявляли значительную противовоспалительную активность.
Как видно из гистограммы, обе лекарственные формы проявляли значительную противовоспалительную активность.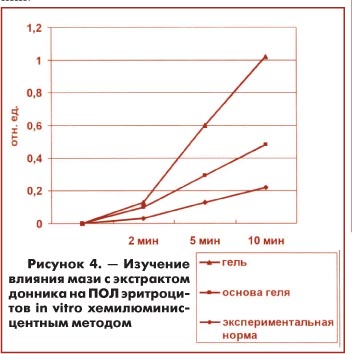 Мазь с экстрактом донника лекарственного (традиционная) была проверена на наличие и степень ранозаживляющей активности. Изучение прооксидантного действия in vivo на модели перекисного гемолиза эритроцитов крыс, индуцированного перекисью водорода хемилюминесцентным методом и заживление линейной кожной раны (Убашев И.Ю. и соавт., 1990). Изучение прооксидантного действия показало, что исследуемая мазь повышала уровень перекисного окисления на 106,6% (р<0,01) на 10-ой минуте эксперимента по сравнению с контролем, которым служил фосфатный буфер.
Мазь с экстрактом донника лекарственного (традиционная) была проверена на наличие и степень ранозаживляющей активности. Изучение прооксидантного действия in vivo на модели перекисного гемолиза эритроцитов крыс, индуцированного перекисью водорода хемилюминесцентным методом и заживление линейной кожной раны (Убашев И.Ю. и соавт., 1990). Изучение прооксидантного действия показало, что исследуемая мазь повышала уровень перекисного окисления на 106,6% (р<0,01) на 10-ой минуте эксперимента по сравнению с контролем, которым служил фосфатный буфер.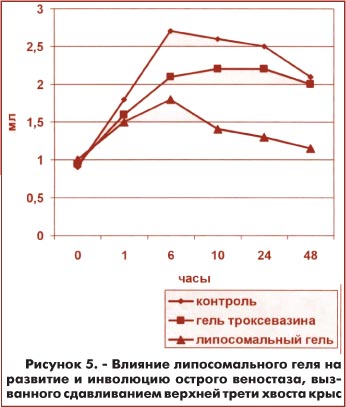 Далее на основе экстрактов донника и лавра была разработана технология геля на липофильной основе, содержащего комплекс биологически активных веществ, таких как хлорофилл, кумарины, тритерпеноиды, каротиноиды, фенольные соединения. Технология липосомального геля выполнялась традиционно. Оказалось, что полученный гель обладает широким спектром фармакологической активности и может быть рекомендован для лечения травматических отеков и отеков, вызванных веностазом. Исследования проведенные в сравнении с 2% гелем троксевазина на моделях травматического отека задней лапки крысы ( Lim К., Rink К. et all, 1961) и острого веностаза путем наложения лигатуры на верхнюю треть хвоста крысы (Nordmann H.I. и др., 1984) на белых крысах-самцах показали, что липосомальный фитогель донника тормозил развитие и ускорял инволюцию острого венозного застоя, превышая при этом результаты действия препарата сравнения. Результаты регистрировались онкометрически по приросту объёмов поврежденных конечностей.
Далее на основе экстрактов донника и лавра была разработана технология геля на липофильной основе, содержащего комплекс биологически активных веществ, таких как хлорофилл, кумарины, тритерпеноиды, каротиноиды, фенольные соединения. Технология липосомального геля выполнялась традиционно. Оказалось, что полученный гель обладает широким спектром фармакологической активности и может быть рекомендован для лечения травматических отеков и отеков, вызванных веностазом. Исследования проведенные в сравнении с 2% гелем троксевазина на моделях травматического отека задней лапки крысы ( Lim К., Rink К. et all, 1961) и острого веностаза путем наложения лигатуры на верхнюю треть хвоста крысы (Nordmann H.I. и др., 1984) на белых крысах-самцах показали, что липосомальный фитогель донника тормозил развитие и ускорял инволюцию острого венозного застоя, превышая при этом результаты действия препарата сравнения. Результаты регистрировались онкометрически по приросту объёмов поврежденных конечностей.